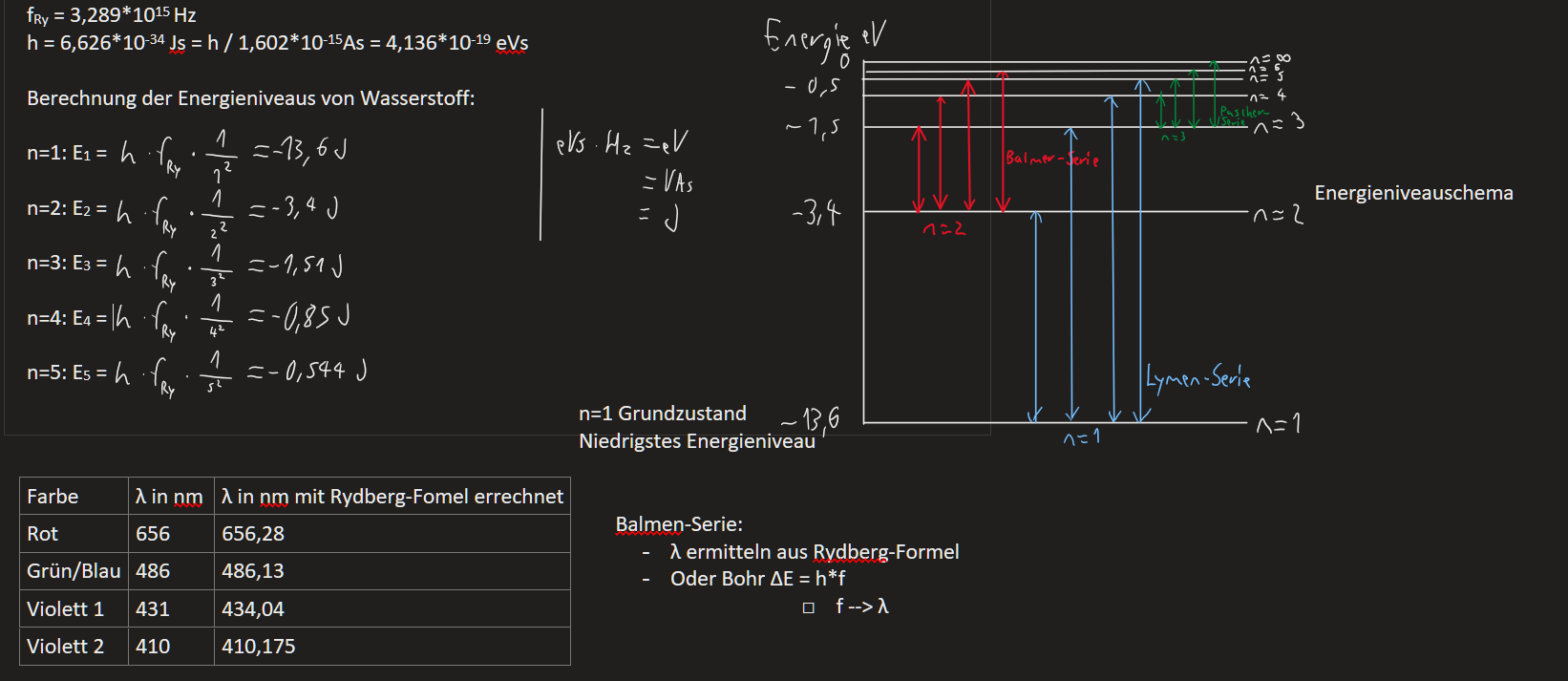
Berechnung des Frequenzspektrums von Wasserstoff
1885 Balmer
… : Rydbergfrequenz …: 3,4,5,6 Balmer Serie
1888 Rydberg
| m=1 | Lyman-Serie | UV-Bereich |
|---|---|---|
| m=2 | Behman-Serie | sichbarer-Bereich |
| m=3 | Paschen-Serie | Infrarot-Bereich |
| m=4 | Brackett-Serie | Infrarot-Bereich |
Bohr:
- Jede Spektrallinie des Wasserstoffatoms entspricht einem Energiebetrag,
Wasserstoffatom im Bohrschen-Atommodell:
- laufen auf stabilen Bahnen um den Kern mit einer bestimmten Energie
- Beim Übergang zwischen 2 Energieniveaus wird ein Photon emittiert | absorbiert: